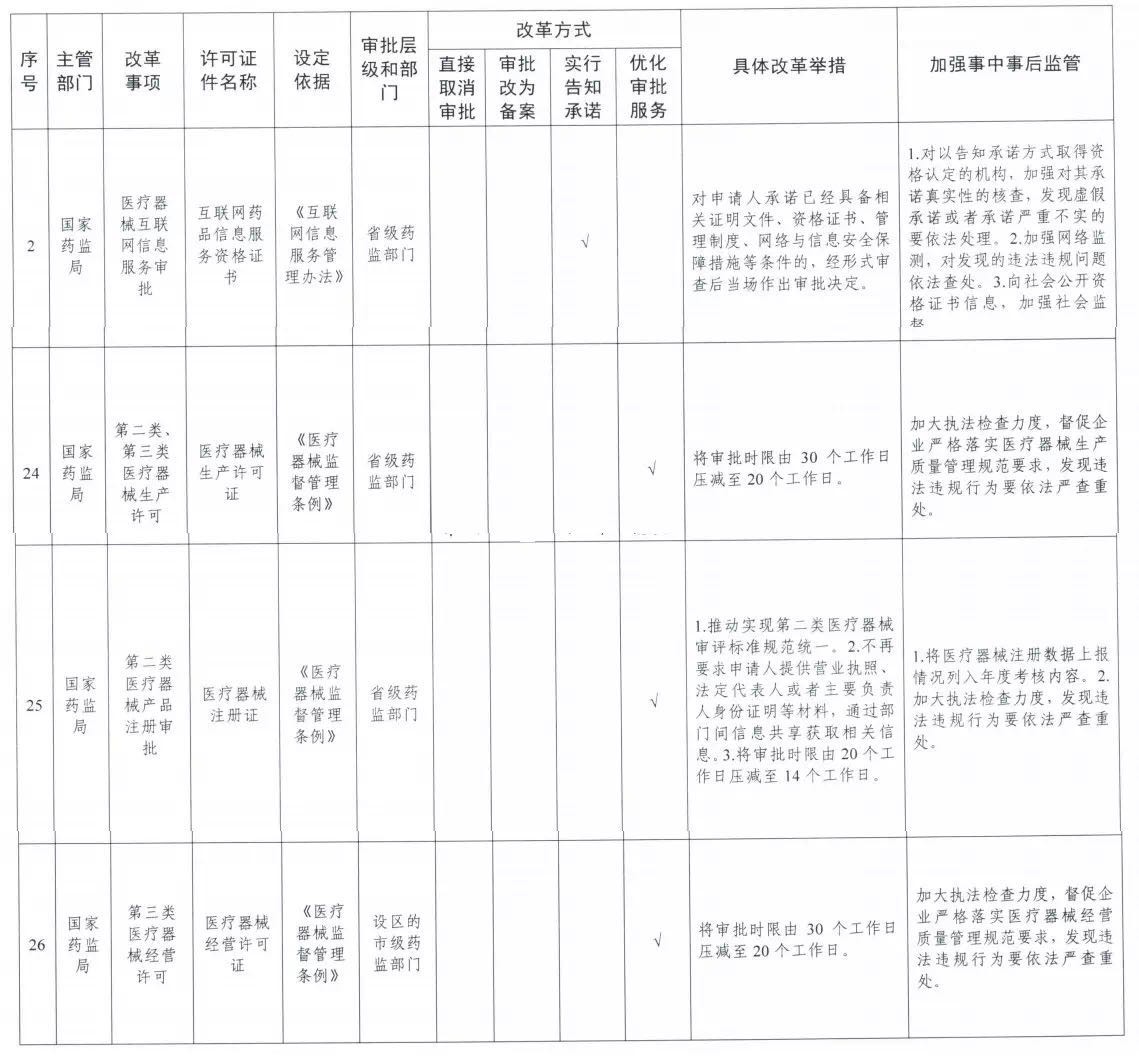
今日,药监局发布了《国家药品监督管理局贯彻落实国务院在自由贸易试验区开展“证照分离”改革全覆盖试点实施方案》,试点范围扩大至18个省,将对一批行政审批事项进行改革,主要为优化审评流程、压缩审评时间。其中涉及到医疗器械的如下:
国家药监局关于印发《国家药品监督管理局贯彻落实国务院在自由贸易试验区开展“证照分离”改革全覆盖试点实施方案》的通知
上海、广东、天津、福建、辽宁、浙江、河南、湖北、重庆、四川、陕西、海南、山东、江苏、广西、河北、云南、黑龙江省(自治区、直辖市)药品监督管理局,局机关各司局、各直属单位:
现将《国家药品监督管理局贯彻落实国务院在自由贸易试验区开展“证照分离”改革全覆盖试点实施方案》印发给你们,请结合工作实际,认真贯彻落实。
国家药监局
2019年11月27日
国家药品监督管理局贯彻落实国务院在自由贸易试验区开展“证照分离”改革全覆盖试点实施方案
为贯彻落实《国务院关于在自由贸易试验区开展“证照分离”改革全覆盖试点的通知》(国发〔2019〕25号,以下简称25号文件)要求,全面扎实推进药品监管领域“证照分离”改革各项工作,制定本方案。
一、指导思想
以习近平新时代中国特色社会主义思想为指导,全面贯彻党的十九大和十九届二中、三中、四中全会精神,按照党中央、国务院决策部署,持续深化“放管服”改革,进一步明晰政府和企业责任,全面清理药品监管领域涉企经营许可事项,分类推进审批制度改革,完善简约透明的行业准入规则,进一步扩大药品、医疗器械、化妆品企业经营自主权,创新和加强事中事后监管,优化营商环境,激发市场活力,推动产业高质量发展。
二、试点范围和内容
自2019年12月1日起,在上海、广东、天津、福建、辽宁、浙江、河南、湖北、重庆、四川、陕西、海南、山东、江苏、广西、河北、云南、黑龙江等自由贸易试验区,对药品监管领域涉企经营许可有关事项按照实行告知承诺、优化审批服务两种方式推进改革,为在全国实现“证照分离”改革全覆盖形成可复制可推广的制度创新成果。改革试点涉及药品监管领域许可事项共28项(见附件),其中实行告知承诺的许可事项3项,优化审批服务的许可事项25项。
三、分类推进审批制度改革
(一)明确3项实行告知承诺事项的监管制度。对“药品互联网信息服务审批”“医疗器械互联网信息服务审批”“医疗机构使用放射性药品(一、二类)许可”3项事项,各试点地区省级药品监管部门依据《互联网药品信息服务管理办法》规定的许可条件和核发放射性药品使用许可证验收标准,于11月30日前依法准确完整列出可量化可操作、不含兜底条款的许可具体条件,明确事中事后监管措施和违反承诺的后果,制作告知承诺书示范文本。(试点地区省级药品监管部门负责)
(二)按实行告知承诺方式开展审批。12月1日试点启动后,各试点地区省级药品监管部门要严格按照实行告知承诺的方式开展“药品互联网信息服务审批”“医疗器械互联网信息服务审批”“医疗机构使用放射性药品(一、二类)许可”事项的审批服务,一次性告知企业许可条件、事中事后监管措施,以及违反承诺的后果,制定或更新办事指南,提供告知承诺书示范文本。申请企业作出承诺并按要求提交材料后,各试点地区省级药品监管部门经形式审查作出许可决定,相关条件符合要求的,准予许可并当场核发《互联网药品信息服务资格证书》《放射性药品使用许可证》,相关条件不符合要求的,要当场一次性告知需要补充材料。作出审批决定后,要依法及时向社会公开审批证书有关信息,便利公众查询,加强社会监督。因审批部门未按规定告知造成的损失,由有关审批部门承担。(试点地区省级药品监管部门负责)
(三)明确2项审批权限下放事项的办理程序。为方便企业就近办事,12月1日起,“放射性药品生产企业审批”和“放射性药品经营企业审批”事项的审批权限由国家药监局和国家国防科工局下放至试点地区省级药品监管部门和省级国防科技工业部门。各试点地区省级药品监管部门应当参照国家药品监管局公布的放射性药品生产、经营企业审批办事指南等相关规定,于11月30日前制定公布准确完备、简明易懂的办事指南,明确申报程序、完善工作标准、细化部门职责,做好直接受理“放射性药品生产企业审批”和“放射性药品经营企业审批”事项的各项准备工作。国家药监局尽快会同相关部门制定出台审批相关工作要求。(试点地区省级药品监管部门、国家药监局药品监管司分别负责)
(四)做好审批权限下放事项的衔接落实。12月1日起,各试点地区省级药品监管部门应依法进行放射性药品生产、经营企业审批,规范自由裁量权,严格时限约束,消除隐形门槛,持续加强人员培训。作出审批决定后依法及时向社会公开审批证书有关信息,便利公众查询,加强社会监督。下放审批权限后,国家药品监管局要加强对试点地区省级药品监管部门的人员培训和业务指导,适时开展督查,密切关注出现的新问题,及时解决纠正。做好下放行政许可事项的落实和衔接,确保下放的许可事项放得开、接得住、管得好。(试点地区省级药品监管部门、国家药监局药品监管司分别负责)
(五)更新23项优化审批服务事项的办事指南。为提高审批效率,降低办事成本,12月1日起,对“药品生产企业许可”“化妆品生产许可”“第二类、第三类医疗器械生产许可”等23项许可事项采取精简审批材料、优化办事流程、压减审批时限等措施优化审批服务。试点许可事项涉及的药品监管部门应及时制定、更新办事指南并于11月30日前向社会公开。(国家药监局受理和举报中心、药品注册司、药品监管司,试点地区省级药品监管部门,试点地区市、县级人民政府负责药品监管的部门分别负责)
(六)落实优化审批服务事项的改革举措。试点许可事项涉及的药品监管部门要按25号文件所列具体改革举措,对“药品生产企业许可”等可事项,精简许可条件和审批材料,坚决取消“奇葩证明”。对“化妆品生产许可”等事项,采取申请、审批全程网上办理的方式优化办理流程。对“国产药品再注册审批”等事项,采取关联现场检查的方式优化办理流程,进一步提高审批效率。对“第二类、第三类医疗器械生产许可”等可事项,压减审批时限。(国家药监局药品注册司、药品监管司,试点地区省级药品监管部门,试点地区市、县级人民政府负责药品监管的部门分别负责)
四、完善改革配套措施
(一)加强事中事后监管。按照“四个最严”要求,充分运用检查、检验、监测等手段,加强日常监督管理,依法查处虚假承诺、非法经营等违法违规行为,督促企业持续依法合规经营。在监管过程中,发现虚假承诺或承诺严重不实的,责令企业限期整改,逾期不改或整改后仍达不到要求的,依法撤销许可证件,依照相关法律法规规定,在一定时限内不予受理相应许可申请。虚假承诺或违反承诺造成的损失由企业自行承担。
(二)创新监管工作模式。应将通过告知承诺获取许可的企业与通过一般审批程序获证的企业平等对待。对审批权限下放的事项,推动完善药品监管、国防科工、生态环境等部门间的协调配合机制,及时共享相关信息。按照信用监管要求,加强对检查结果的运用,对守信企业实行联合激励、对失信企业实施联合惩戒。进一步强化社会监督,依法及时处理投诉举报。注重发挥行业协会作用,引导社会力量积极参与市场秩序治理。
(三)持续提高服务水平。深入推进审批服务标准化,规范自由裁量权,严格时限约束,消除隐形门槛。加快推进“互联网+政务服务”,推动涉企经营许可事项从申请、受理到审核、发证全流程“一网通办”、“最多跑一次”。加强对审批行为的监督管理,建立审批服务“好差评”制度,由企业评判服务绩效。
(四)坚持依法有序推进改革。根据法律法规的调整情况,及时对规章、规范性文件作出相应调整,适时出台对地方实施改革比较统一明确的指引文件,为顺利进“证照分离”改革全覆盖试点提供制度支撑。试点工作推进过程中,遇到新情况、新问题,要及时组织研究并报告。
(五)做好过渡期的受理审批工作。各试点地区省级药品监管部门于12月1日起依法受理试点地区的“放射性药品生产企业审批”和“放射性药品经营企业审批”申请。对12月1日前国家药品监管部门已受理的试点地区“放射性药品生产企业审批”和“放射性药品经营企业审批”申请,由国家药品监管部门继续审批。对12月1日前已受理、尚未完成审批的其余26项事项,试点许可事项涉及的药品监管部门应按照25号文件所列具体改革举措办理。
五、切实抓好改革政策落实
(一)强化组织领导。开展“证照分离”改革,是落实党中央、国务院重大决策部署,持续优化营商环境,释放企业创业创新活力的重要举措。试点许可事项涉及的药品监管部门要高度重视,将改革工作列入重要议事日程,加强组织领导,及时研究解决工作中的重大问题,保证各项工作取得实效。
(二)狠抓工作落实。试点许可事项涉及的药品监管部门要上下联动、密切配合,以钉钉子的精神全面抓好改革任务落实,严格按照国务院文件要求,不折不扣执行到位,落实责任、跟踪问效,确保各项改革举措落到实处。
(三)加强宣传解读。“证照分离”改革试点政策量大面广,要组织做好改革试点政策的宣传解读,扩大政策知晓度,让企业准确感知改革的力度和温度,为改革试点顺利推进营造良好氛围。