对腹腔内置疝修补补片动物实验设计的考量
一、前言
临床前动物实验研究是医疗器械安全性和有效性综合评价的重要组成部分,特别是需临床试验审批医疗器械、创新性医疗器械、罕见病和临床急需医疗器械、对于需要解剖而人体临床无法开展研究的产品等,临床前动物实验可能不可或缺。对于医疗器械是否需要开展临床前动物研究,申请人需根据产品作用原理、产品设计及材料的创新程度、非临床研究的充分性、动物实验研究目的等方面综合考虑以做出判断。
本文以腹腔内置疝修补补片产品为例,就为何开展临床前动物实验及实验设计的要素进行论述,相关内容来源于我中心已组织制订的《腹腔内置疝修补补片动物实验技术审查指导原则》,该技术文件已面向公众广泛征集意见,并与中华医学会外科学分会疝和腹壁外科学组临床专家、动物实验机构专家进行专题研讨后完成修订,现已向医疗器械注册管理司送审。
二、腹腔内置疝补片开展临床前动物实验的必要性
由于任何异物置入人体腹腔都有可能与腔内组织器官发生粘连[1],进而可能引起严重的并发症,因此,考察疝修补补片置入腹腔后发生粘连的可能性及粘连程度是评价产品安全性的重要因素。在产品进行临床研究前,一方面需要开展动物实验以保护临床受试者的安全,另一方面考虑到临床试验中很难直接观察到补片在人体内的粘连情况,所以必须开展相关动物实验,对补片与腔内组织器官的粘连情况、新生腹膜的情况进行评价,以控制产品上市后肠瘘、肠梗阻、肠粘连等相关并发症的风险。
三、腹腔内置疝补片临床前动物实验的要素
以下内容主要针对腹腔内置的不可吸收补片、不可吸收材料与预期可降低粘连的材料层复合制备而成的补片。其它类型的腹腔内置补片产品,可根据产品具体情况参考。相关要素反映了对补片与腔内组织间粘连情况有关动物实验研究的基本要求。对于新材料、新设计的腹腔内置疝补片,申请人宜根据产品特性开展更深入的动物实验研究,如需选择多个种属的实验动物、增加观察时间点、选择相应的统计学方法等。另外需注意,当考虑同时对产品有效性和安全性相关的多个项目进行综合性评价时,例如对修补组织的机械性能、腹壁的组织学、补片皱缩情况、移位情况、生物相容性等项目进行评价,动物实验设计要素可能会与本文存在差异。
(一)动物种类及模型
选择适用的实验动物进行补片粘连情况的动物实验研究。申请人需对动物实验中所采用动物的适用性进行分析,提供动物种类选择及模型建立的确定依据,如参考文献或前期探索性动物实验资料等。
考虑到实验动物与人体在腹壁解剖结构、新生腹膜化程度等方面的可比性,建议选择一定数量的某种成年大型动物(如小型猪、比格犬)进行动物实验研究。动物实验最终采用病理解剖的方式进行评价。若实验过程中采用腹腔镜方法进行连续观察,则不应对粘连位置进行操作,避免对后续结果的评价造成影响。实验中使用的补片尺寸建议至少为5cm×5cm。
动物实验中宜对补片进行固定,并保证补片完全贴合腹壁。
(二)对照的选择
宜选择材质、结构设计方面最相似的境内已上市产品作为动物实验的对照器械。在开展新生腹膜的组织学观察结果评价时建议与自然腹膜进行比较。考虑随机化的设计并予以描述。
(三)评价指标的选择
1.评价粘连情况的指标
评价补片与腹腔内组织器官的粘连情况时建议对粘连强度、粘连面积分别评价,并对两个量化指标进行综合评价。
表1补片与腹腔内组织器官的粘连情况评价表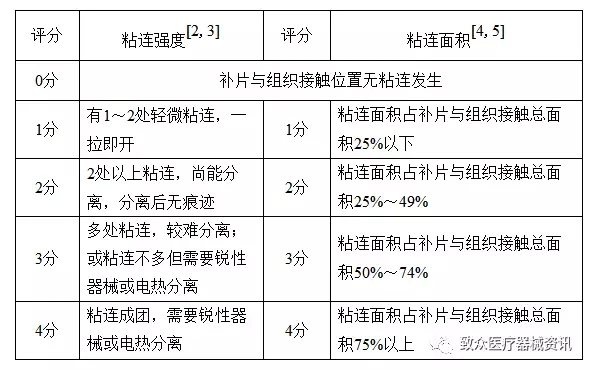
表2粘连情况综合评价表
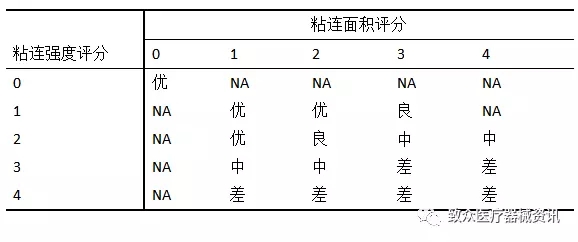
综合评价的复合指标为粘连情况的优良率,粘连情况优良即为临床可接受的粘连情况,公式如下:

2.评价新生腹膜情况的指标
以组织学分析手段进行新生腹膜情况的评价,推荐的评价方法如下:取材范围包括整个植入区连同周围1cm正常腹壁,取材深度包括整个植入区组织连同其覆盖的腹膜,将取材标本沿同一对角线方向切开后取连续组织块依次分别切片后做病理检查[6,7]。通过鉴定间皮细胞层形成评价新生腹膜的情况,需对连续切片中的“修复区表面间皮细胞层长度/修复区长度”比值进行统计分析。
注:对于膨体聚四氟乙烯等合成材料制备的致密补片,该项指标不适用。
3.动物实验中与产品安全性及有效性相关的其它指标
如并发症及不良反应情况、生物组织学反应等。
(四)观察时间点的选择
制定动物实验观察点时需考虑选择的动物模型种类、产品的降解/吸收周期、粘连及新生腹膜形成的关键时期[8]等因素,并提供合理的确定依据。
对于产品腹腔一侧为不可吸收材料的产品,观察时间点宜选择至少28天[9]。对于产品腹腔侧为可吸收材料的产品,根据产品预期完全降解的时间确定观察时间点[10,11]。
(五)实验样本量及结果分析
1.样本量
一般情况下,动物实验样本量需结合实验目的、设计类型、评价指标及评价方法的准确性、试验器械及对照器械的情况、实验用动物的变异性、外科手术操作的一致性、实验中动物的预期损耗率、分析数据所用的统计学方法等因素来综合确定,并需有统计学考虑。可将现有的实验数据作为确定样本量的参考,包括文献报道的动物实验或申报产品的预实验情况。申请人应在注册资料中提交动物实验样本量的确定依据,鉴于实验动物的变异性较小,建议完成有效实验的植入试验器械及对照器械的动物样本量均不少于10只。
2.结果分析
定量指标的统计描述将计算均值、标准差、中位数、最小值、最大值,下四分位数(Q1),上四分位数(Q3);分类指标的统计描述各类的例数、发生率及构成比。
动物试验若采用单只动物双侧分别植入实验产品及对照产品的设计,要分析实验组比对照组结果更好或者相当的比率和可信区间(可用精确概率法得出),另外可分别报告实验组比对照组结果更好的比率及两组结果相当的比率。提供实验组与对照组的优良率差值及其可信区间并考虑组间相关性。
动物试验若采用单只动物分别植入实验产品或对照产品的设计,对两组一般情况的比较将根据指标的类型采用适当的方法进行分析,定量资料的组间比较采用成组t检验或Wilcoxon秩和检验,分类数据采用卡方检验或精确概率法;等级资料采用Wilcoxon秩和检验。提供实验组与对照组的优良率差值及其可信区间。
动物实验结论需包括统计学分析与生物学数据分析的综合评价结果。
(六)其它需关注的问题
为保证动物实验结果真实、可靠,应使用质量合格的实验动物或检疫合格的实验用动物。建议在具备动物实验资质(如:有关部门颁发的动物实验资格证明文件)的机构开展动物实验。申请人需与动物实验实施单位签订合同并共同设计、制订动物实验方案,上述资料作为产品质量体系管理文件存档。注册时提交申请人与动物实验实施单位共同确认并签章的动物实验报告,另外建议提供动物实验实施单位的资质文件。
为保证动物实验的研究质量,应尽量避免不同术者手术操作差异、动物麻醉死亡、手术死亡、术后感染及其它意外情况对产品评价产生影响。建议申请人邀请有经验的经过培训的专业人员进行评价。申请人需保存详细的实验情况记录及分析资料,包括以下适用的内容:所有受试品及对照品信息、动物饲养记录、镇痛麻醉记录、手术过程记录、原始病理照片、手术切片、手术录像等实验原始资料、对动物麻醉死亡等非预期事件的有关证据及分析资料等。为了保证数据的溯源性,上述资料需作为产品质量管理体系文件存档。