(防疫产品,如医用口罩,防护服,隔离衣,新冠病毒检测试剂盒)上诉防疫产品,需要什么样的ce认证和fda认证?如何辨别ce认证和fda认证的有效性?
|
产品名称 |
预期用途 |
上市途径 |
|
防护口罩 |
用于保护佩戴者,颗粒物防护,防止过敏、感染,避免伤害 |
按PPE法规进行CE认证 |
|
医用口罩 |
用户保护患者或者医疗专业人员,用于易传染、卫生保健或手术环境中 |
无菌口罩:按MDR法规进行CE认证 非无菌口罩:按MDR法规进行自我宣称 |
|
一般防护服 |
用于保护穿着者,防止伤害 |
按PPE法规进行CE认证 |
|
医用防护服 |
医疗专业人员,用于手术或感染环境中 |
无菌隔离衣:按MDR法规进行CE认证 非无菌隔离衣:按MDR法规进行自我宣称 |
|
新冠病毒检测试剂盒 |
用于新冠病毒检测使用,在专业医疗检测机构使用。 |
按IVDD法规进行自我宣称 |


新冠病毒检测试剂盒的CE认证资料:
http://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.main

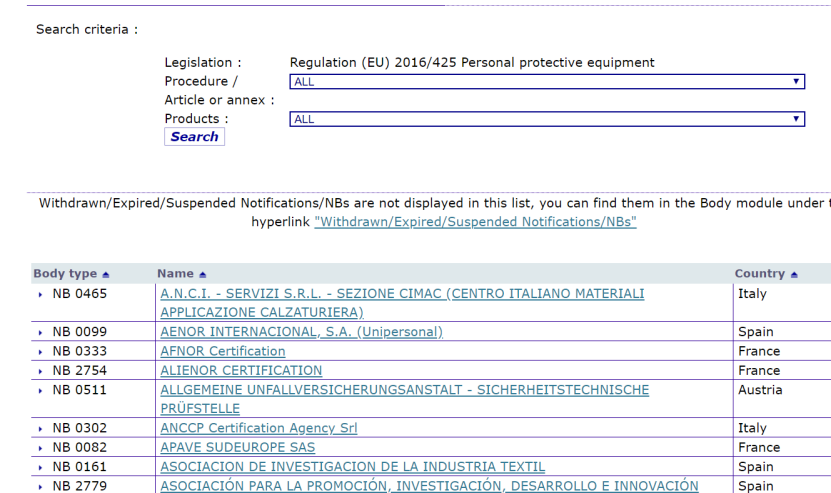
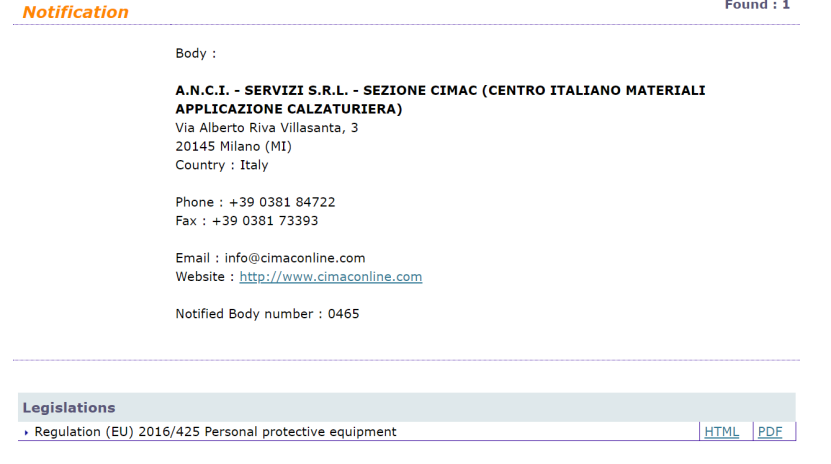
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=notification.pdf&dir_id=155501&ntf_id=279842
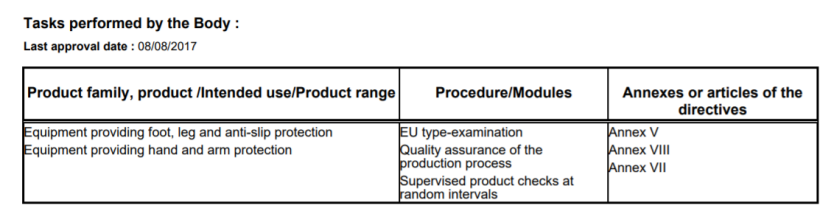
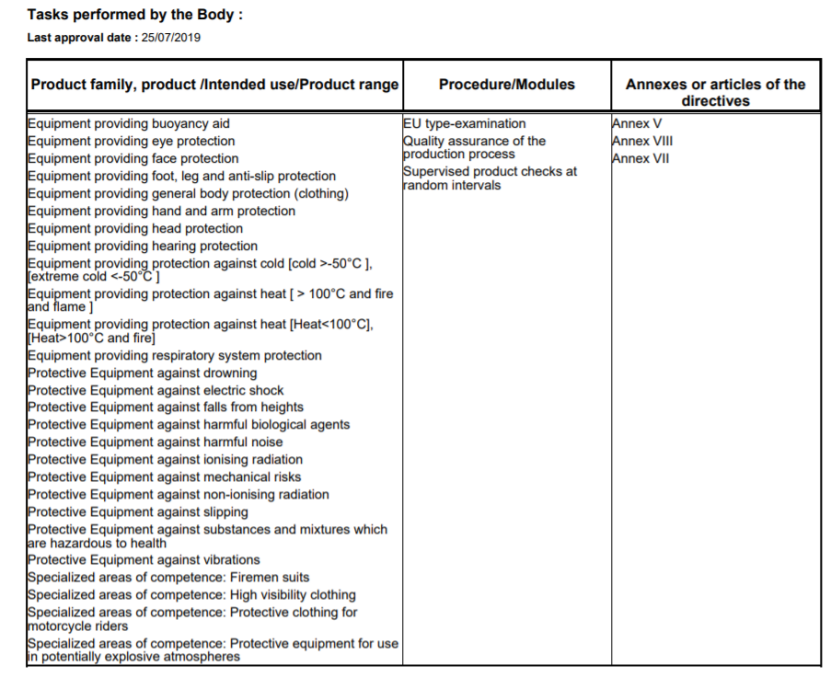
二、问题中提到的防疫物资在美国也是有不同的法规来管理,主要有以下种类:
|
产品类别 |
过滤效率 |
|
N95 |
过滤至少95%的空气传播颗粒,不耐油。 |
|
Surgical N95 |
经NIOSH批准的N95呼吸器,也已被美国食品药品管理局FDA批准作为手术口罩。 |
|
N99 |
过滤至少99%的空气传播颗粒,不耐油。 |
|
N100 |
过滤至少99.97%的空气传播颗粒,不耐油。 |
|
R95 |
过滤至少95%的空气传播颗粒,有点耐油。 |
|
P95 |
过滤至少95%的空气传播颗粒,极耐油。 |
|
P99 |
过滤至少99%的空气传播颗粒,极耐油。 |
|
P100 |
过滤至少99.97%的空气传播颗粒,极耐油。 |
NIOSH-Approved Particulate Filtering Facepiece Respirators
https://www.cdc.gov/niosh/npptl/topics/respirators/disp_part/default.html
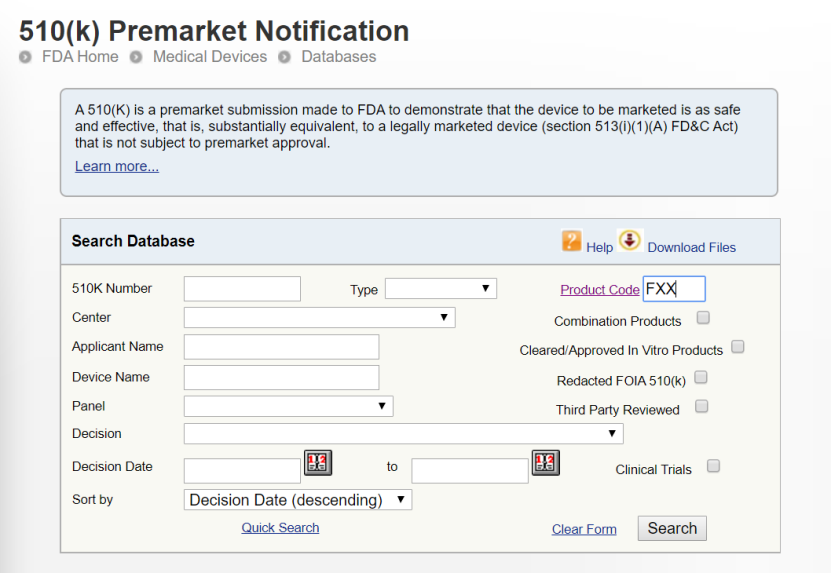
经过美国FDA注册的医用口罩,可以在FDA官网上查询到相关信息。
|
产品代码 |
器械 |
Regulation number |
器械分类 |
提交形式 |
|
FXX |
Mask, Surgical 外科口罩 |
|
II |
510(k) |
|
OXZ |
Pediatric/Child Facemask 儿科/儿童口罩 |
|
II |
510(k) |
|
OUK |
Surgical Mask With Antimicrobial/Antiviral Agent 外科口罩带抗菌剂/杀菌剂 |
|
II |
510(k) |
|
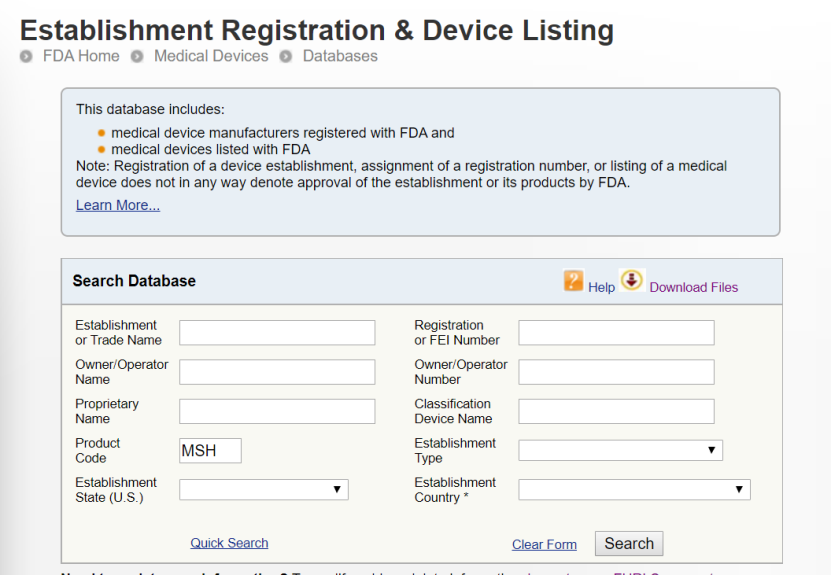
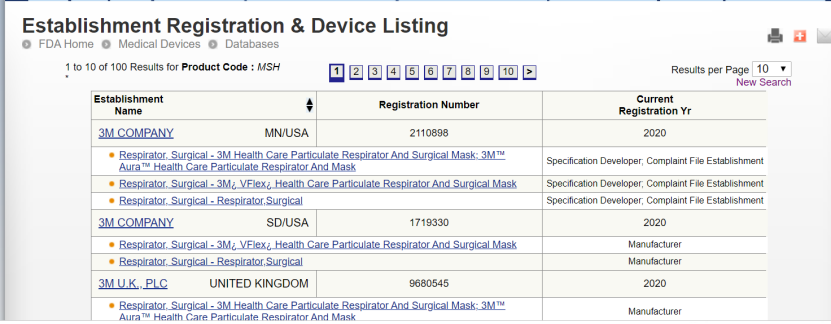
MSH |
Respirator, Surgical 外科呼吸器具 |
|
II |
510(k) Exempt 510(k)豁免 |
|
ONT |
N95 Respirator With Antimicrobial/Antiviral Agent N95口罩,带抗菌剂/杀菌剂 |
|
II |
510(k) |
|
NZJ |
Respirator, N95, For Use By The General Public In Public Health Medical Emergencies N95口罩,供一般市民在公共卫生及医疗紧急事故中使用 |
|
II |
510(k) |
|
ORW |
N95 Respirator With Antimicrobial/Antiviral Agent For Use By The General Public In Public Health Medical Emergencies N95口罩,带抗菌剂/杀菌剂,供一般市民在公共卫生及医疗紧急事故中使用 |
|
II |
510(k) |

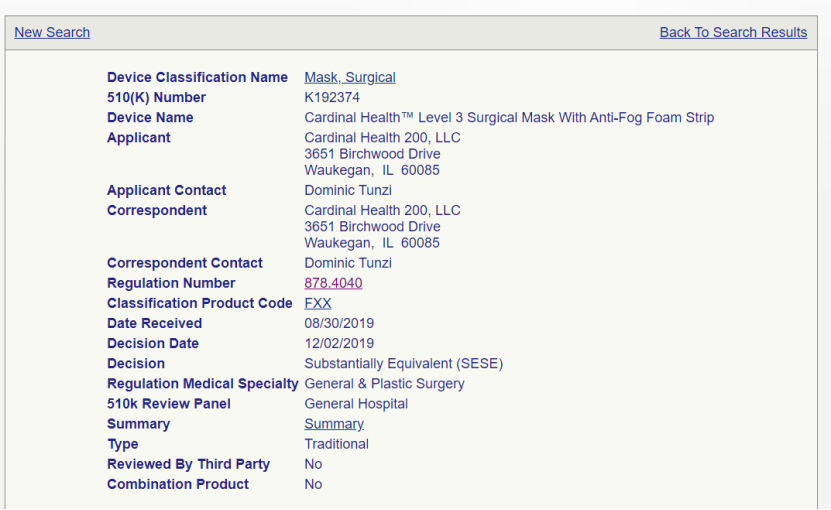
https://www.accessdata.fda.gov/cdrh_docs/pdf19/K192374.pdf
https://www.fda.gov/medical-devices/emergency-situations-medical-devices/emergency-use-authorizations#coronavirus2019

本文系原创,未经授权请勿转载
下一篇:【原创】医疗器械检测7问7答