近日,江西省食品药品监督管理局发布了一批20家医疗器械经营企业飞行检查情况的通报,值得注意的是,其中江西金禾生物科技有限公司竟然拒绝接受飞行检查,该企业在飞检组老师明确告知飞检事项后,仍未到现场配合检查,并且不再接听飞检组老师的电话。
对此,南昌市局要依据《医疗器械监督管理条例》、《药品医疗器械飞行检查办法》等有关规定对江西金禾生物科技有限公司拒绝接受飞行检查的行为依法处理。
按照《药品医疗器械飞行检查办法》,企业拒绝、逃避飞检的,应由检查组书面记录、并责令改正,经责令改正后仍不改正、造成无法完成检查工作的,检查结论判定为不符合相关质量管理规范或者其他相关要求。
此外,如果企业有拒绝、逃避检查情形,又因违法行为应当受到行政处罚的,将由药监从重处罚。
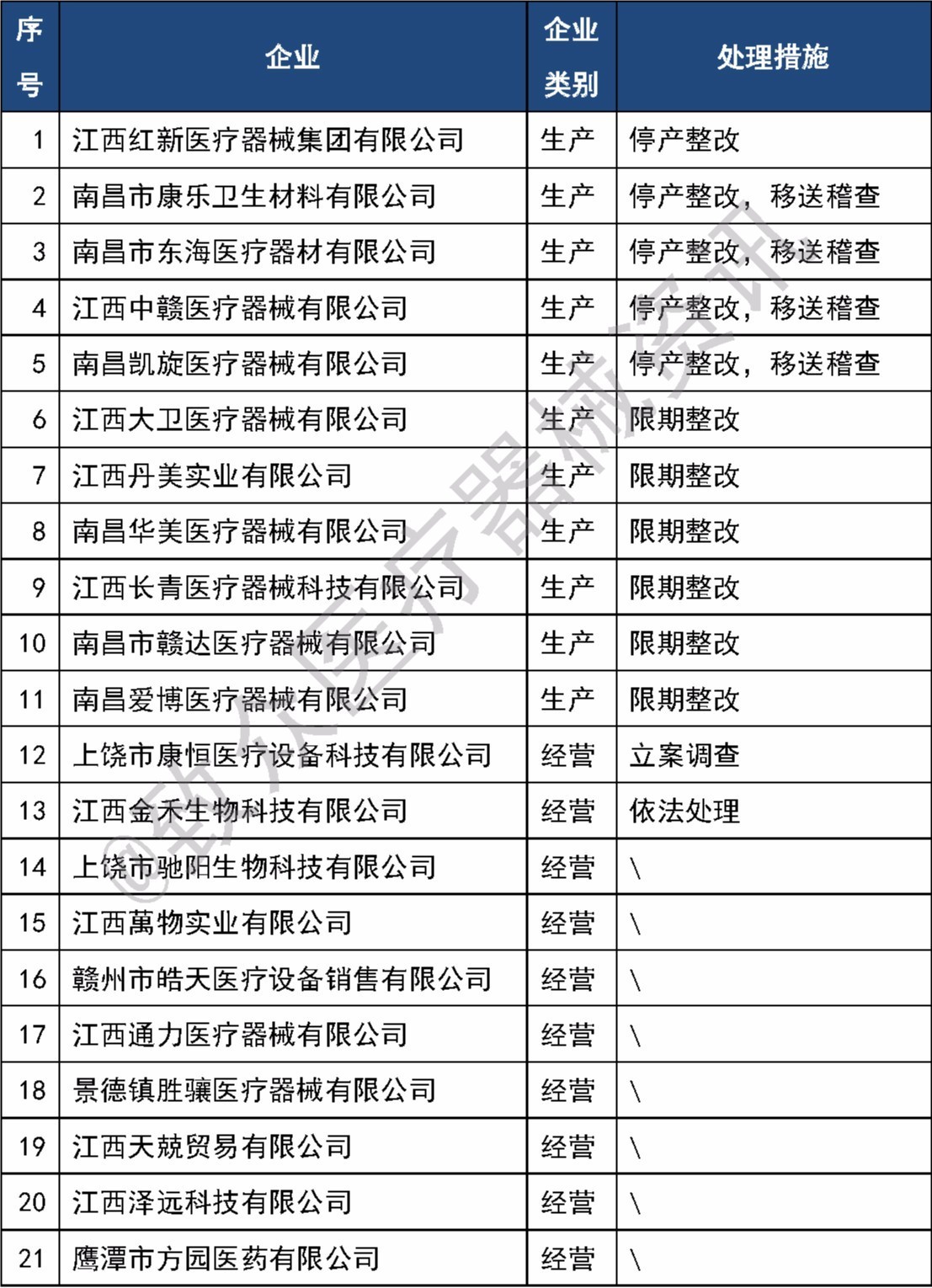
自2017年5月9日至今,江西省食品药品监督管理局共发布了3批医疗器械企业飞行检查的通报,涉及31家医疗器械相关企业,其中,11家为生产企业,5家被责令停产整改,并有4家移送稽查,其余20家为经营企业。以下是部分已公开的21家企业飞检信息表:
以下是本次20家经营企业飞行检查情况通报原文:
关于2017年开展部分医疗器械经营企业飞行检查情况的通报
各设区市食品药品监督管理局,樟树药品监督管理局,省食品药品稽查局:
为进一步加强医疗器械流通领域监管,规范医疗器械经营行为,督促企业提升质量管理水平。2017年7月3日至7日,省局在全省范围内组织开展了部分医疗器械经营企业飞行检查。现将有关情况通报如下:
一、基本情况
按照《关于抽调人员参加医疗器械监督检查的通知》(食药监械函〔2017〕6号)的要求,抽调21名医疗器械检查员,组成10个检查组,采取交叉检查方式,分别对南昌、上饶各3家,九江、赣州、吉安、宜春各2家,其余设区市(含樟树市)各1家,共20家医疗器械批发或批零兼营企业进行了飞行检查,检查范围覆盖全省各地市。重点检查经营条件是否与许可审批时一致;需要冷藏、冷冻医疗器械的冷链管理是否符合规定;查验产品是否从正规渠道购进;是否存有销售无注册证、超过有效期产品的现象;是否违规从事互联网医疗器械经营等。
通过飞检发现,全省各地市局重视医疗器械流通领域监管工作,加强日常监管,加大医疗器械违法违规行为打击力度,医疗器械经营企业法制意识逐步增强,经营行为逐步规范,管理水平逐步提升。同时,检查中也发现不少问题,仍存在违法违规经营行为或不符合医疗器械经营质量管理规范要求等现象。
二、存在的主要问题
1.存在未经许可从事医疗器械经营活动的行为。上饶市康恒医疗设备科技有限公司于2017年3月15日取得《医疗器械经营许可证》和《第二类医疗器械经营备案凭证》,在2017年3月15日前存在有未经许可从事医疗器械经营活动的行为。
2.拒绝接受飞行检查。江西金禾生物科技有限公司在检查组多次电话联系企业法人都无人接听或挂断,直至9:30企业法人才接听了检查组拨过去的电话,检查组再次明确告知飞行检查相关规定,要求企业在10:02之前派人来现场配合检查,企业法人在电话里答应立即派人在约定的时间内来检查现场,直到10:07企业未派人到现场接受检查,检查组又再次拨打企业法人的电话,能够接通,但不接听,拒绝接受飞行检查。
3.存在“空壳公司”现象。上饶市驰阳生物科技有限公司、江西萬物实业有限公司、赣州市皓天医疗设备销售有限公司等三家企业原注册经营地址大门紧闭,人去楼空。
4.擅自改变原许可审批的经营条件。江西通力医疗器械有限公司擅自变更经营地址和仓库地址;景德镇胜骧医疗器械有限公司擅自扩大经营范围;江西天兢贸易有限公司经营条件发生变化,不再符合医疗器械经营质量管理规范要求;江西泽远科技有限公司存在与其他企业共用仓库的现象;鹰潭市方园医药有限公司存在与其他企业共用冷库的现象。
5.质量负责人不在岗。检查发现企业质量负责人不在岗问题比较突出,许可审批时符合资质条件的质量负责人已离职离岗,无人履行质量管理职责。
6.需低温冷链管理的医疗器械管理不规范等问题。少数体外诊断试剂经营企业冷链设施设备不能满足储运要求,无法提供相关记录。
7.购销记录内容不完整。个别企业未建立购进、销售记录;未使用计算机管理系统,无法做到产品可追溯。
三、有关要求
(一)省食品药品稽查局要对上饶市康恒医疗设备科技有限公司未经许可从事医疗器械经营活动的违法经营行为予以立案调查,依法处理;南昌市局要依据《医疗器械监督管理条例》、《药品医疗器械飞行检查办法》等有关规定对江西金禾生物科技有限公司拒绝接受飞行检查的行为依法处理。
(二)各地要高度重视,对飞检中发现的问题,要求企业限期整改,开展跟踪检查,督促整改到位;对整改不到位,要及时采取措施;对存在违法违规问题的企业,要及时依法查处;对“空壳公司”要及时履行注销程序。
(三)各地要结合监管实际,进一步加强医疗器械经营企业监管,严厉打击违法经营行为,规范流通领域经营秩序,确保医疗器械产品安全有效。
(四)请各有关单位于2017年 9月30日前将处理结果报省局医疗器械监管处。省局将适时实地抽查各地依法处理情况。
联系人:赵宋云
联系电话:0791-88158033
邮编:330029,地址:江西省南昌市北京东路1566号。
江西省食品药品监督管理局
2017年8月22日
(公开属性:主动公开)
来源:江西省食品药品监督管理局
整理:TACRO
【声明】部分文章和信息来源于互联网,不代表本订阅号赞同其观点和对其真实性负责。如转载内容涉及版权等问题,请立即与我们联系(杨 13260664005),我们将迅速采取适当措施