2017年5月15日,FDA在其官网上发布了关于其监管事务办公室(Office of Regulatory Affairs, ORA)项目整合(Program Alignment)的最新消息。
近年来,FDA监管的产品越来越复杂,市场更加广阔,规范相关机构行为的规则更为复杂化。为了应对这些挑战,FDA需要不断调整其运作模式,以提高维护公众健康的能力。FDA的项目整合计划酝酿已久,2013年9月,即由时任局长启动,旨在全面整合人力资源,以跟上科学创新加速、市场全球化以及新的项目任务的步伐。预期此次改革后,FDA工作人员的技术领域专业化程度将进一步提升,同时还进一步优化工作流程,以明确职责,促进跨部门沟通、加强协作。
ORA整合项目的主要内容是对相关检查机构的组织架构进行重组,从原来基于地域为主的管理架构调整为基于产品领域为主的项目结构。重组后,同一检查员不再像原来一样,承担既检查食品企业又检查药品企业的任务。
ORA新的组织架构如图1所示。在此次改革之前,ORA分为五个大区和20个区域办公室。此次经过整合后,ORA主要设立七个以产品为核心的管理部门(见图1蓝色部分):
☆ 生物研究监测运营办公室
☆ 生物制品运营办公室
☆ 医疗器械和放射健康运营办公室
☆ 药品质量运营办公室
☆ 执法和进口运营办公室
☆ 烟草运营办公室
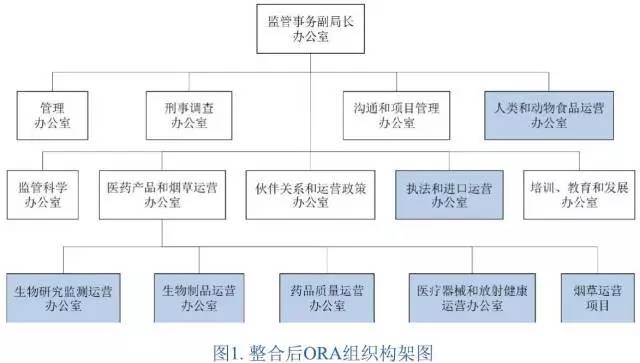
除了烟草运营办公室,其他六个管理部门还进一步细划职能,分由几个大区进行管理。
此外,ORA的实验室也将基于产品领域进行整合。
FDA声明,此次整合并不会关闭任何区域办公室,也不会有员工被辞退或调整工作区域。
FDA认为,通过此次整合,可以使ORA能够更好地对FDA监管的产品开展检查活动,并更好地使ORA与FDA内部其他部门(如CDER)进行对接,优化协作,减少重复工作,提高监管效率。
来源:CFDI检查核查之窗
整理:致众TACRO
【声明】部分文章和信息来源于互联网,不代表本订阅号赞同其观点和对其真实性负责。如转载内容涉及版权等问题,请立即与我们联系(杨 13260664005),我们将迅速采取适当措施