一、检查频次及覆盖率要求
根据国家食药监总局《医疗器械经营企业分类分级监督规定》(食药监械监〔2015〕58号),现针对不同类别的检查频次及覆盖轨要求。
(一)针对“无菌类、植入材料和人工器官类、体外诊断试剂、设备仪器类等实施三级监管的医疗器械经营企业,及医疗器械进口总代、经营需冷链储运产品企业、上年度存在行政处罚,及存在不良信用记录的企业”,各区市场监管局每年检查不少于一次。
(二)针对“角膜接触镜类和计划生育类三级监管企业”,各区可视辖区监管情况监管频次适当调整,但年度监管频次最低不得低于该类企业总数的35%。对二级监管的经营企业,各区市场监管局日常检查频次不低于二级监管企业总数的50%,对一级监管的经营企业日常检查频次不低于一级监管企业总数的35%。
(三)针对“企业从事网上医疗器械交易行为”,各区市场监管局应将纳入日常监管内容,实行线上线下一体化管理,监管频次与企业的分级监管频次相同。
(四)针对“为其他医疗器械生产经营企业提供贮存、配送的经营企业”,市局组织每年检查不少于一次。
此外,各级监管部门可根据监督检查动态情况、质量抽验、投诉举报等情况以及监管对象的质量管理风险水平,适当增加检查频次。(责任部门:药械流通处、局认证审评中心、各区市场监管局;配合部门:执法总队)
二、四类专项检查要求
根据国家总局年度例行工作要求,结合我市近年药械化流通质量风险梳理情况,结合日常监管工作,2017年开展至少下列四类专项检查。
(一)装饰性彩色平光隐形眼镜专项检查。根据《国家食品药品监管总局办公厅关于严厉打击非法经营装饰性彩色平光隐形眼镜行为的通知》(食药监办械监〔2015〕48号)要求,开展医疗器械彩色平光隐形眼镜经营企业年度监督专项检查,并于11月15日前上报专项检查总结及专项检查报表(附表1)。(责任部门:各区市场监管局)
(二)避孕套质量安全专项检查。根据《食品药品监管总局关于加强避孕套质量安全管理的通知》(食药监械监〔2015〕30号)要求,结合日常监管工作,开展避孕套经营企业监督检查,并于11月15日前上报专项检查总结及专项检查报表(附表2)。(责任部门:各区市场监管局)
(三)无菌和植入医疗器械专项检查。根据《食品药品监管总局办公厅关于加强无菌和植入性等医疗器械监督检查的通知》(食药监办械监〔2017〕10号)要求,结合日常监管,开展无菌和植入医疗器械经营、使用监督检查,并于11月15日前上报专项检查总结及专项检查报表(附表3)。(责任部门:各区市场监管局)
(四)医疗器械免费体验店专项检查。依据《关于进一步加强免费体验医疗器械行为监管的通知》(沪食药监药械流〔2015〕299号),重点查处以免费体验为名,夸大产品疗效、虚假宣传、搭配销售为实的免费体验医疗器械行为。专项检查方案由各区市场监管局自行制定,并于11月15日前上报专项检查总结及专项检查报表(附表4)。(责任部门:各区市场监管局)
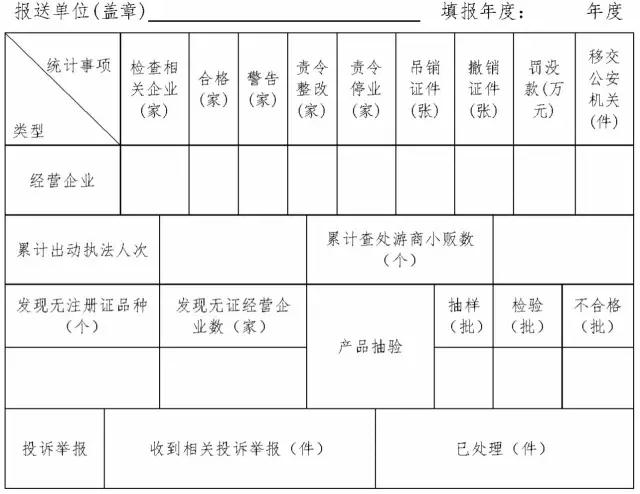
附表1
装饰性彩色平光隐形眼镜专项检查汇总表

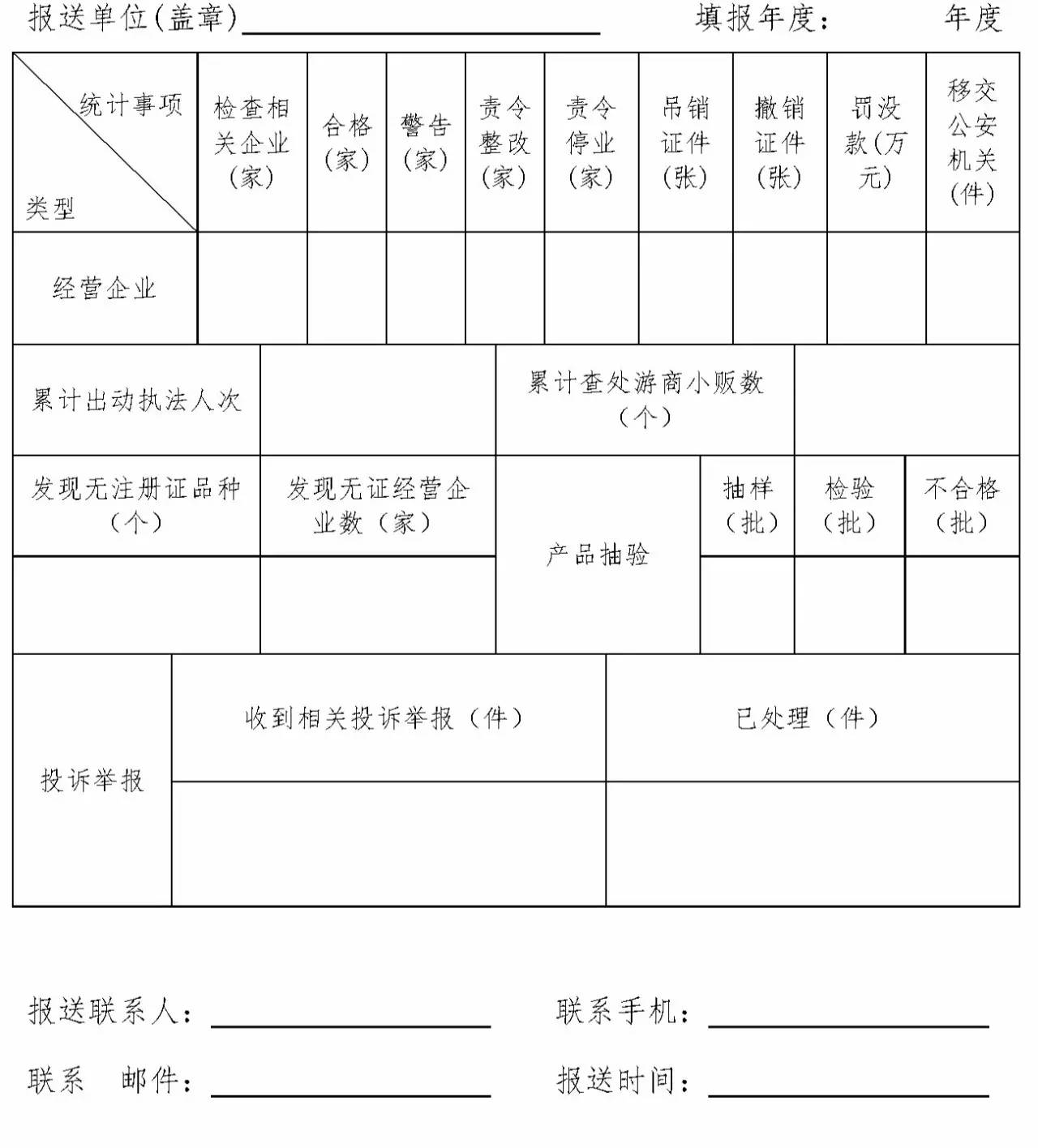
附表2
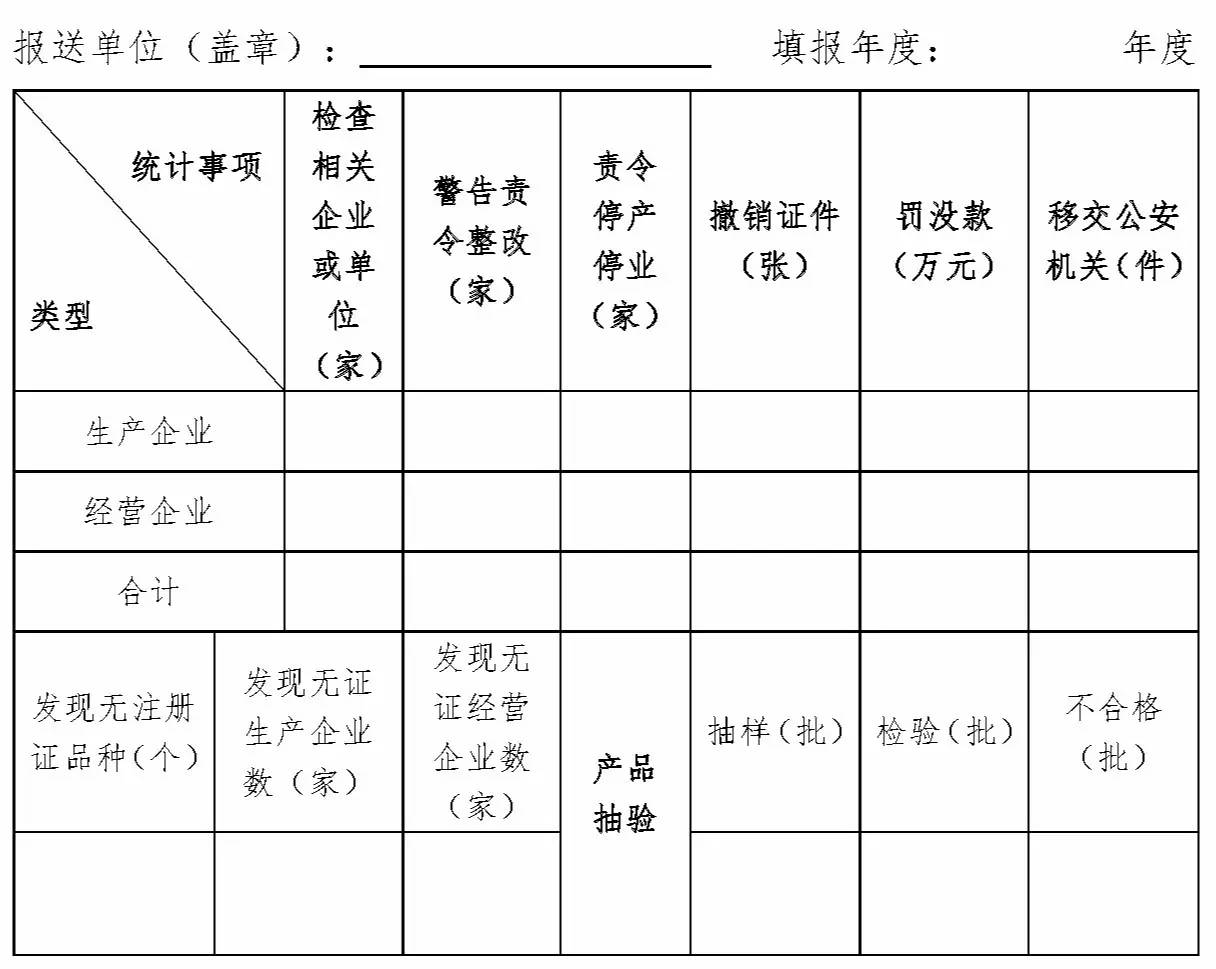
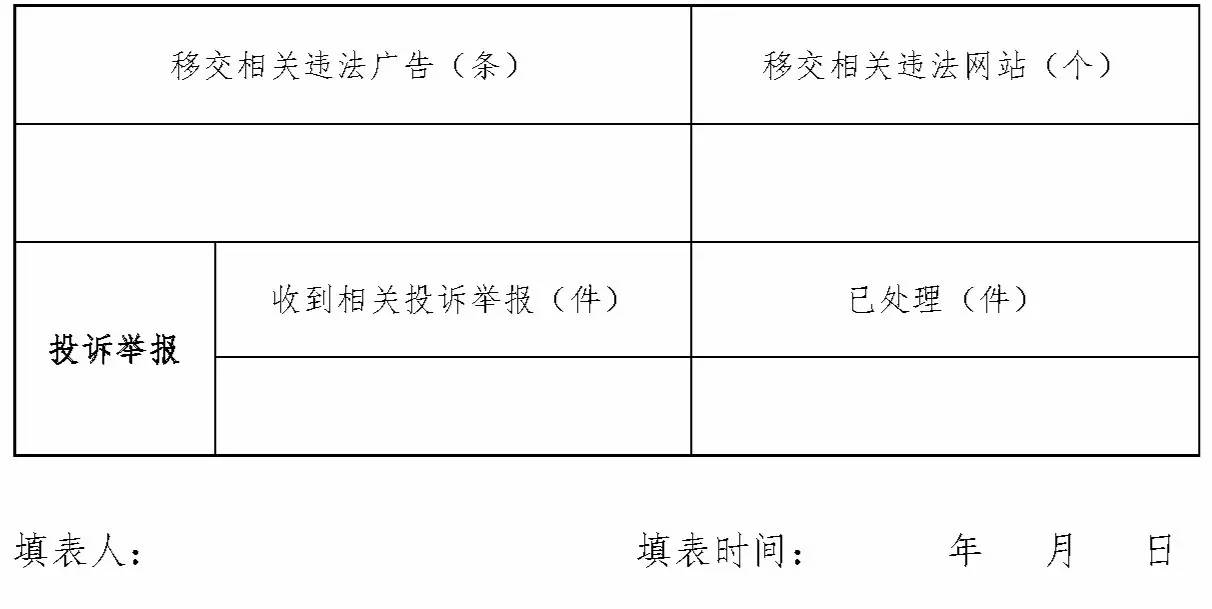
加强避孕套质量安全管理工作统计表
附表3
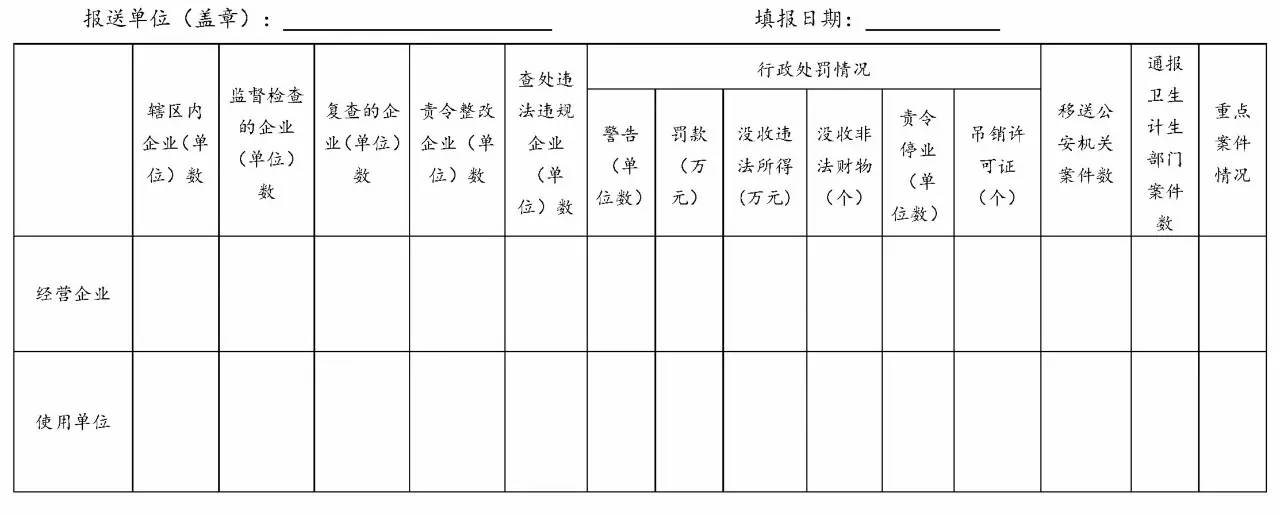
2017年无菌和植入性医疗器械经营使用单位监督检查情况统计表
附表4
医疗器械免费体验店专项检查汇总表
来源:上海市食品药品监督管理局
整理:TACRO
【声明】部分文章和信息来源于互联网,不代表本订阅号赞同其观点和对其真实性负责。如转载内容涉及版权等问题,请立即与我们联系(杨 13260664005),我们将迅速采取适当措施